Rev. OFIL 2017, 27;1:61-66
Fecha de recepción: 07/01/2016 – Fecha de aceptación: 20/09/2016
____
Recuero Galve L1, Mulet Alberola AM2, Sánchez Gundín J1, Mejía Recuero M2, Marcos Pérez G2, Barreda Hernández D3
1 Licenciada en Farmacia. Residente de Farmacia Hospitalaria
2 Licenciada en Farmacia. Especialista en Farmacia Hospitalaria
3 Licenciada en Farmacia. Jefe de Servicio
Servicio de Farmacia. Hospital Virgen de la Luz. Gerencia de Atención Integrada de Cuenca (España)
____
Correspondencia:
Lidia Recuero Galve
Hermandad Donantes de Sangre, s/n
16002 Cuenca
Correo electrónico: lidiarega@gmail.com
____
Resumen
Objetivo: Evaluar efectividad, seguridad y grado de satisfacción de pacientes con esclerosis múltiple (EM) en tratamiento con fampridina.
Métodos: Estudio observacional descriptivo prospectivo (octubre 2013-abril 2014) en un hospital de segundo nivel. Se revisó historia farmacoterapéutica (Farmatools®) e historia clínica electrónica (MambrinoXXI®) de los pacientes en tratamiento. Se evaluó: efectividad mediante el test de la marcha de 25 pasos (T25FW) inicial y tras 14 días; seguridad: estudio de las reacciones adversas medicamentosas (RAM) experimentadas por los pacientes; grado de satisfacción con el medicamento: cuestionario Treatment Satisfaction Questionnaire for Medication (TSQM) (versión 1.4).
Resultados: 24 pacientes (18 mujeres) iniciaron fampridina. Edad media: 48,8±8,3 años. Efectividad: T25FW inicial 23,55±12,26 segundos y 17,82±8,50 segundos tras 14 días. 2 mujeres con EM remitente recurrente y escala EDSS 4 y 6 respectivamente, suspendieron tratamiento por falta de mejoría de la marcha. Seguridad: 10 pacientes no experimentaron RAM. RAM más frecuentes: estreñimiento (4 pacientes), insomnio y cefalea (3 pacientes), mareo, ansiedad y aumento de transaminasas (2 pacientes). Supusieron la suspensión en 5 pacientes. 18 pacientes realizaron la encuesta, obteniéndose una satisfacción global (SG) con el medicamento de 11,6±3,3 (Puntuación Máxima Posible 17).
Conclusiones: Fampridina demostró efectividad, disminuyendo 6 segundos el T25FW en el 81,5% de los pacientes y con una valoración satisfactoria en TSQM. Las RAM supusieron la suspensión del tratamiento en 20,8% de la población, sin experimentar ninguna en el 41,6% de los pacientes. La SG con el medicamento fue elevada (11,6 vs. 17) por lo que el tratamiento cumplió las expectativas de los pacientes.
Palabras clave: Fampridina, esclerosis múltiple, satisfacción del paciente.
____
Introducción
La esclerosis múltiple (EM) es una enfermedad neurológica crónica inflamatoria, desmielinizante y discapacitante que afecta al sistema nervioso central (SNC). Conlleva importantes repercusiones personales, sociales y económicas para el paciente y su entorno1,2.
La EM es la segunda causa de discapacidad en adultos jóvenes tras los accidentes de tráfico. En general, afecta más a las mujeres que a los hombres (2:1 de los casos)1. La edad de inicio predominante es entre 30-32 años y la prevalencia en nuestro medio es entre 60 y 100 casos por cada 100.000 habitantes2.
Existen diferentes formas de manifestación de la enfermedad: EM remitente recurrente (EMRR), EM progresiva secundaria (EMPS), EM progresiva recidivante (EMPR) y EM progresiva primaria (EMPP). La EMRR es la más común (afecta a más del 80% de los pacientes)3,4.
El tratamiento se puede subdividir en 3 categorías: tratamiento modificador de la enfermedad (TME), tratamiento de los brotes de la enfermedad y tratamiento sintomático5.
El TME está encaminado a reducir el número de recaídas, la severidad de las lesiones y frenar el curso progresivo de la enfermedad. En la actualidad existen 9 fármacos aprobados como agentes modificadores de la enfermedad: interferón beta 1a y beta 1b, acetato de glatirámero, mitoxantrona, natalizumab, fingolimod, teriflunomida y dimetilfumarato5.
El tratamiento de exacerbaciones de la enfermedad se realiza con altas dosis de corticoides, generalmente de metilprednisolona 500-1000 mg/día durante 3 a 10 días5.
El tratamiento sintomático ayuda a mejorar la calidad de vida, aunque no siempre mejora muchos de los síntomas que presenta el paciente, ya que estos no responden a la terapia farmacológica5.
Los síntomas que padecen los pacientes con EM son consecuencia de la desmielinización y la pérdida axonal progresiva del SNC, que conllevan deterioro neurológico y originan con frecuencia discapacidad y minusvalia6. Los más frecuentes son: dolor, espasticidad, espasmos, fatiga, depresión, trastornos motores, visión borrosa, disfagia y trastornos del sueño6,7.
La espasticidad se define como resistencia al estiramiento muscular pasivo causado por una exageración del tono secundaria a una desinhibición central del arco reflejo miotático7. Se ha estimado que aproximadamente un 80% de los pacientes padecen espasticidad y entre el 30-50% de estos tienen un grado de moderado a severo8. En muchos enfermos la espasticidad es responsable de la fatigabilidad inducida por el movimiento y de la alteración del sueño (por los espasmos y por la dificultad para moverse en la cama durante la noche).
El objetivo del tratamiento de la espasticidad ha sido eliminar o evitar factores que la pueden incrementar, como son: infecciones, estreñimiento, dolor, fiebre y úlceras por presión principalmente; y corregir o evitar las posturas que la incrementan. Para todo ello, tradicionalmente se han utilizado combinaciones de medidas farmacológicas y rehabilitadoras. Entre las medidas farmacológicas, los fármacos por vía oral utilizados para la espasticidad han sido los siguientes:7
– Baclofeno: tratamiento de elección en la espasticidad generalizada y espasmo. Es un agonista del receptor GABA-B que actúa produciendo inhibición de la actividad de las motoneuronas gamma y disminuyendo la sensibilidad de los músculos espinales, reduciendo así la espasticidad y los calambres7,9.
– Tizanidina: agonista de receptores α-2-adrenérgicos que actúa inhibiendo la acción de la sustancia P en la médula espinal dorsal, causando efecto analgésico y reduciendo los espasmos7,9.
– Benzodiazepinas: actúan suprimiendo los impulsos sensoriales desde los músculos y receptores cutáneos, potenciando la acción del GABA e inhibiendo las vías descendentes excitatorias. La más utilizada ha sido el diazepam, aunque también se han utilizado otros como el clonazepam. Su principal inconveniente es la sedación que produce al utilizarlas a altas dosis para que tenga efecto antiespasmódico7,9.
– Dantroleno sódico: relajante muscular de acción periférica7,9.
Por vía parenteral, se puede utilizar la toxina botulínica para administración local. Actúa bloqueando la liberación de acetilcolina en la unión neuromuscular, produciendo por tanto una denervación química transitoria. Además, puede desempeñar un papel analgésico al inhibir la liberación periférica de neurotransmisores nociceptivos. Constituye el tratamiento de elección en la espasticidad focal y complementario en la generalizada9.
Baclofeno y tizanidina se utilizan en primera línea de tratamiento de la espasticidad. Ante la no respuesta a estos tratamientos, se puede utilizar delta-9-tetrahidrocannabinol-cannabidiol que está indicado para pacientes con EM con espasticidad moderada o grave que no han respondido a medicamentos antiespasmódicos10.
La disfunción motora con o sin debilidad es uno de los síntomas más incapacitantes en los pacientes con EM. Puede deberse a la afectación de diferentes sistemas descendentes: tracto corticobulbar, corticoespinal, cerebeloso y vías sensitivas, a las que se añade la fatiga y la motivación7. Son síntomas primarios que aparecen en el 50% de los pacientes con EM. Presentan un curso temprano de la enfermedad y producen debilidad de la marcha, espasticidad, ataxia y trastornos sensoriales. Una de las consecuencias más graves de la aparición de espasticidad es la dificultad para andar que junto con la reducción de la movilidad, es un trastorno muy frecuente que impacta de forma muy negativa en pacientes con EM. Las opciones de tratamiento recomendadas han sido medidas de terapia física y ayudas de tipo ortopédico, que pueden implicar un estigma adicional. Los TME pueden estabilizar parcialmente la progresión del deterioro de la marcha, aunque en general no mejoran su disfunción11. Sin embargo, en enero 2012 se aprobó por la Agencia Española del Medicamento, un nuevo fármaco, fampridina, un bloqueante de los canales de potasio, de administración oral. La introducción de fampridina, supone el estándar actual para el tratamiento de trastornos de dificultad de la marcha en pacientes diagnosticados de EM, puesto que es el único tratamiento autorizado para mejorar la marcha en personas adultas con EM11-13.
Fampridina es un medicamento con registro de uso hospitalario. Su mecanismo de acción consiste en el bloqueo de los canales de potasio dependientes de voltaje, disminuyendo la pérdida de K+, por lo tanto, aumentan los potenciales de acción y la conducción, y potencia la trasmisión sináptica y neuromuscular de la señal nerviosa. Presenta farmacocinética lineal, con absorción completa a nivel del aparato digestivo, siendo esta absorción más lenta que la de su metabolito activo, 4-aminopiridina de liberación inmediata. Por ello, se presenta como comprimidos de liberación prolongada que presentan un retraso en la absorción de fampridina, manifestado por un aumento más lento de la concentración máxima más baja, disminuyendo así la aparición de efectos adversos. La pauta posológica de fampridina es 1 comprimido de 10 mg/12 horas11,12.
La prescripción inicial de fampridina se limita a 2 semanas, ya que generalmente los beneficios clínicos deben ser identificados en el plazo de 2 semanas tras comenzar el tratamiento. Se realiza un test de la marcha de 25 pasos (T25FW) antes de iniciar el tratamiento y otro tras las 2 semanas de tratamiento para evaluar la eficacia del mismo. Si no se aprecia mejoría del T25FW se debe suspender el tratamiento con fampridina tal y como se recoge en la ficha técnica12.
Los objetivos de este estudio fueron analizar la efectividad, la seguridad y el grado de satisfacción de pacientes diagnosticados de EM que han iniciado tratamiento con fampridina.
MATERIAL Y MÉTODOS
Estudio observacional descriptivo prospectivo realizado desde el 29 de octubre de 2013 al 15 de abril de 2014 en un hospital de nivel II que atiende a un área asistencial de 146.827 habitantes.
Se incluyeron todos aquellos pacientes que iniciaron tratamiento con fampridina durante el período de estudio. En nuestro hospital, dicho medicamento está incluido en un programa de atención farmacéutica a pacientes en tratamiento para la EM que se desarrolla en la Consulta de Atención Farmacéutica a Pacientes Externos (CAFPE). Mediante la revisión del Módulo de Gestión de Pacientes Externos (Farmatools®) y de la historia clínica electrónica del paciente (MambrinoXXI®) se recogieron los siguientes datos: edad, sexo, escala funcional de discapacidad (EDSS), tipo de EM, TME, tratamientos frente a la espasticidad en uso concomitante con fampridina, duración del tratamiento con fampridina, T25FW y reacciones adversas medicamentosas (RAM). Tras la recogida de datos, en la CAFPE, se procedió a evaluar las siguientes variables:
• Efectividad: se evaluó mediante el T25FW inicial y transcurridos 14 días tras el inicio del tratamiento.
• Seguridad: estudio de las RAM experimentadas por los pacientes y registradas en la historia farmacoterapéutica.
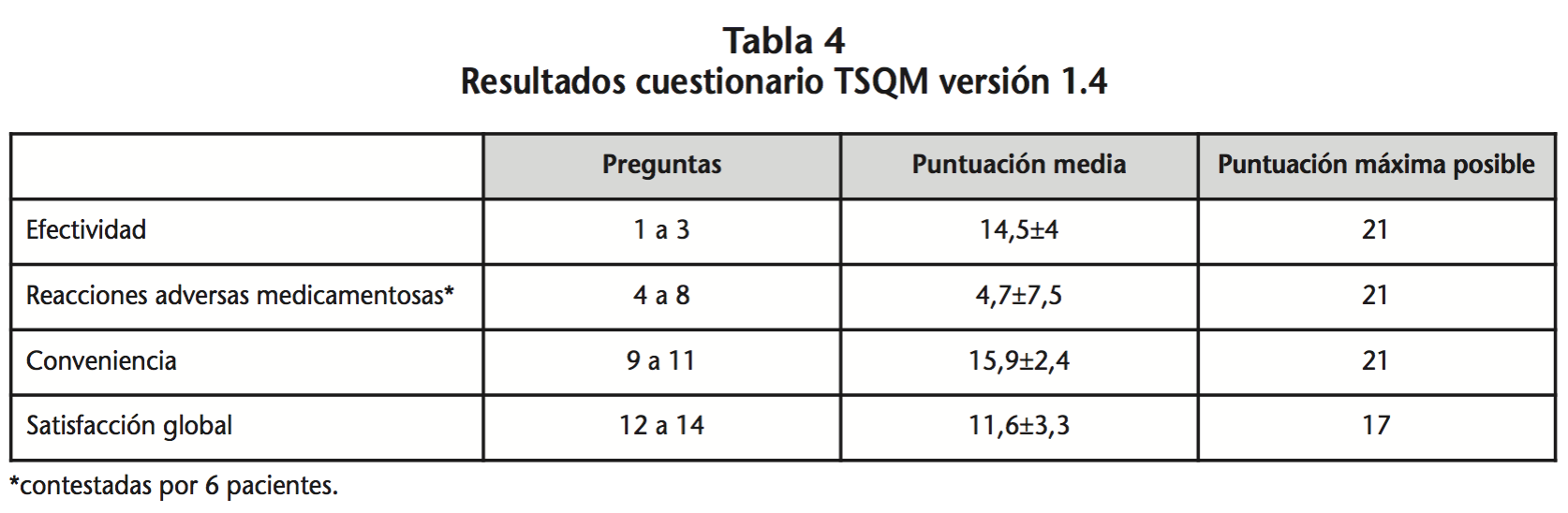
• Grado de satisfacción: para ello se utilizó el cuestionario validado Treatment Satisfaction Questionnaire for Medication (TSQM) (versión 1.4) sobre la satisfacción con el medicamento cuyas preguntas se describen en la tabla 1. Consta de 14 preguntas valoradas mediante escala tipo Likert de 7 puntos (de 1-sumamente insatisfecho a 7-sumamente satisfecho) y clasificadas en 4 categorías: efectividad del tratamiento (preguntas 1 a 3), RAM (preguntas 4 a 8), conveniencia (preguntas 9 a 11) y satisfacción global (preguntas 12 a 14). El cuestionario únicamente se realizó a aquellos pacientes que acudieron a la CAFPE a recoger la continuación del tratamiento tras la primera dispensación. Dicha encuesta se realizó una vez que los pacientes habían iniciado tratamiento con fampridina y acudían a recoger su TME. La CAFPE cuenta con un programa de Atención Farmacéutica a Pacientes con EM con el cual se dispensa a los pacientes medicación para 3 meses. Por tanto, la encuesta se realizó, una vez transcurridos entre 2 y 5 meses tras el inicio con fampridina, haciéndolo coincidir con la dispensación del TME del mes de marzo.
La reducción de la variable de efectividad (T25FW) y una elevada puntuación en el TSQM se consideraron clínicamente relevantes.

RESULTADOS
Durante el período de estudio iniciaron tratamiento con fampridina 24 pacientes, que supone un 28,4% del total de pacientes que reciben medicación dispensada desde el Servicio de Farmacia para el tratamiento de la EM.
Las características iniciales de los pacientes se recogen en la tabla 2 (diferencia por sexo de los pacientes puesto que como se describió en la introducción, la mayor parte de la población afectada fueron mujeres). La duración media del tratamiento con fampridina fue de 88,67±57,32 días [IC95% (64,47-112,87)] hasta cierre del estudio.
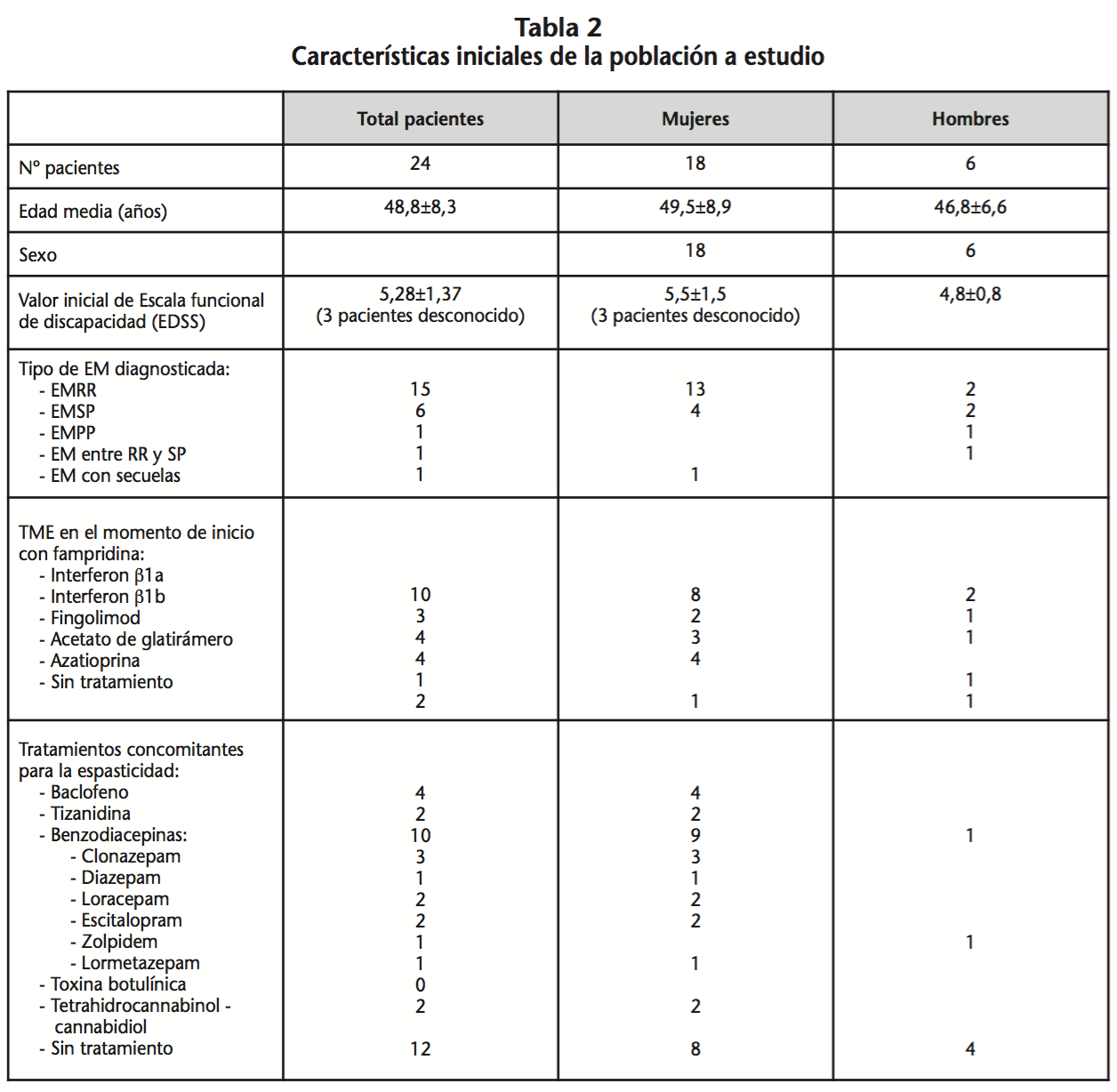
En cuanto a la efectividad, el valor medio inicial del T25FW, medido en los 24 pacientes que iniciaron tratamiento, fue de 23,55±12,26 segundos [IC95% (18,38-28,72)] y a los 14 días de inicio de tratamiento el valor medio, medido en 22 pacientes por no estar registrado el dato en la historia clínica de dos de ellos, fue de 17,82±8,50 segundos [IC95% (14,05-21,59)]. El tratamiento fue suspendido a los 14 días de inicio en 2 mujeres con EMRR y escala EDSS de 4 y 6 respectivamente por falta de mejoría en la marcha (T25FW inicial 23,02 segundos con apoyo y 14 segundos; y T25FW tras 14 días 28,05 segundos sin apoyo y 13 segundos respectivamente).
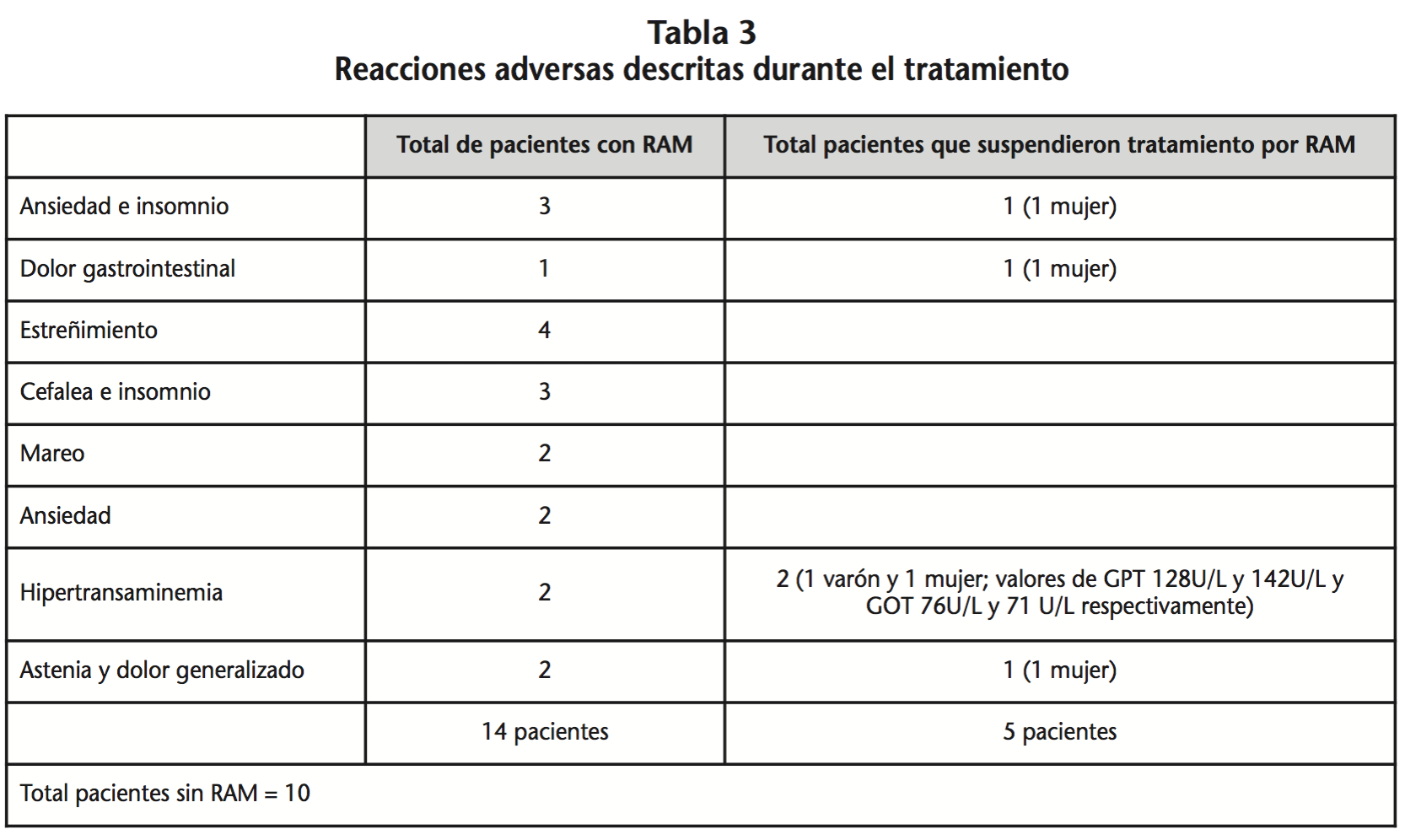
Respecto a la seguridad, de los 24 pacientes que iniciaron fampridina, en 10 pacientes no se detectó ninguna RAM y en 5 pacientes las RAM experimentadas supusieron la suspensión del tratamiento. En la tabla 3 se recogen todas las RAM descritas durante el tratamiento con fampridina y las que supusieron la suspensión del mismo. El tiempo medio hasta suspensión por RAM fue de 60,6±53,8 días [IC95% (-6,2-127,4)].
A cierre de estudio continuaban tratamiento con fampridina 17 pacientes.
La encuesta TSQM versión 1.4 fue realizada a 18 pacientes y los resultados en cada uno de las 4 categorías en las que se encuentra dividida se recogen en la tabla 4.
DISCUSIÓN
La EM es una enfermedad crónica que a largo plazo ocasiona un grado de discapacidad y dependencia importante y limitante para el paciente y su entorno familiar y social. Los TME han demostrado ser eficaces para disminuir el número y la intensidad de los brotes de la enfermedad, pero no consiguen curar la enfermedad, únicamente detener la aparición de brotes. Pese a ello, el avance de la enfermedad va siendo notable, y el empeoramiento de síntomas motores son cada vez más notables para los pacientes2. Hasta el momento, las medidas adoptadas para los problemas de espasticidad desarrollados en el curso de la enfermedad han sido principalmente medidas físicas con la combinación de diferentes tratamientos antispásticos, descritos anteriormente en la introducción, que no han conseguido mejorar los trastornos de la marcha asociados a la espasticidad. Esto ha ocasionado que los pacientes tengan enormes expectativas en la aparición de nuevos tratamientos como fampridina que, además de ser un fármaco oral, actúa disminuyendo ese avance de la enfermedad tan notable en cuanto a la discapacidad motora experimentada por el paciente, de forma eficiente y cumpliendo las expectativas de los pacientes en él5.
En la literatura se han encontrado 2 estudios realizados por Goodman et al., el MS-F203 y MS-F204 que se utilizaron para la aprobación de fampridina. Son 2 ensayos fase III, randomizados, doble ciego y controlados con placebo que evaluán eficacia y seguridad de fampridina. La variable principal de eficacia en ambos estudios fue establecer el número de pacientes respondedores para fampridina y placebo y la mejoría experimentada por los pacientes respondedores en el test de la marcha T25FW. En el estudio MS-F203, de los 301 pacientes incluidos inicialmente, se obtuvieron datos completos de 296 que se aleatorizaron, 224 para el grupo de fampridina y 72 para placebo. Se obtuvo respuesta en el 34,8% del grupo de fampridina frente al 8,3% del grupo placebo. El aumento de velocidad en el test T25FW fue de 26,3% para fampridina versus 5,3% para placebo (p<0,001). En el estudio MS-F204 se analizaron los datos completos de 239 pacientes. De ellos, 118 fueron aleatorizados para el grupo placebo y 119 para fampridina. El 42,9% de los pacientes que tomaron fampridina fueron respondedores frente al 9,3% para el grupo placebo (p<0,001) y en cuanto al T25FW se obtuvo mejoría en el 25,3% para el grupo de fampridina frente a 7,8% en el grupo placebo12,14,15.
Por otro lado, Cameron et al., realizaron un estudio de cohortes con un número de pacientes más similar a nuestro estudio, 39 pacientes. En este estudio, la variable principal de efectividad también fue el T25FW. De los 39 pacientes que iniciaron tratamiento con fampridina, 15 suspendieron tratamiento tras 3 ó 4 semanas después de iniciarlo, en 8 de ellos porque no experimentaron ninguna mejoría. En los 24 restantes se vio una clara mejoría al disminuir el T25FW en 2,7 segundos (p=0,004)16.
Tanto los estudios para la aprobación de este medicamento, como el estudio de cohortes realizado con un número de pacientes más próximo a lo que podemos encontrar en la práctica clínica habitual muestran una clara mejoría en la marcha para los pacientes que han utilizado fampridina. Estos resultados pueden ser comparados con los obtenidos en nuestro estudio donde también se ha observado una clara mejoría con fampridina al disminuir en casi 6 segundos de media el tiempo en realizar el principal test de evaluación, T25FW.
En cuanto a la seguridad, en el ensayo MS-F203, 16 pacientes (7%) en el grupo de fampridina experimentaron una o más RAM, destacando la aparición de trastornos del tracto urinario y brotes de EM. Otras RAM experimentadas fueron mareos, insomnio, fatiga, náuseas, dolor de cabeza o trastornos del equilibrio entre otras. 11 pacientes (5%) en el grupo de fampridina abandonaron el tratamiento ante de finalizar el estudio. Por su parte, en el ensayo MS-F204, 4 pacientes de cada grupo abandonaron el tratamiento antes de finalizar el estudio por RAM y la incidencia de aparición de RAM graves fue de 5 (4,2%) pacientes para fampridina y 3 (2,5%) en el grupo placebo, siendo de nuevo las más destacados los trastornos en el tracto urinario seguido de convulsiones, reflujo gastroesofágico y molestias en el pecho.
Las RAM en nuestro trabajo han supuesto la suspensión del tratamiento en 20,8% de la población y se adecuan al patrón descrito en la ficha técnica, sin experimentar ninguna RAM en el 41,6% de los pacientes, y no siendo una limitación para el paciente, ya que en la encuesta obtienen una valoración muy baja. La satisfacción global con el medicamento es elevada (11,6 vs. 17) por lo que el tratamiento está cumpliendo las expectativas de los pacientes. Indicar ante este último aspecto la existencia de un posible sesgo, ya que la encuesta no se pudo realizar a todos los pacientes que fueron tratados con fampridina.
Por tanto, los resultados obtenidos en nuestro estudio muestran a la fampridina como un tratamiento efectivo, seguro y del cual los pacientes se encuentran satisfechos. Sin embargo, el tamaño muestral del estudio es reducido, hecho que limita el poder sacar conclusiones definitivas.
Ante la expectativa que los pacientes tienen con la llegada de nuevos tratamientos es importante la evaluación de su satisfacción una vez que utilizan estos fármacos. La satisfacción con el tratamiento se define como una evaluación por parte del paciente acerca del proceso de administración del tratamiento y sus resultados relacionados. Se trata de una medida centrada en el paciente que está adquiriendo cada vez más importancia en la práctica clínica ya que, entre otros, podría incidir en el cumplimiento de los regímenes terapéuticos y, por lo tanto, en su efectividad17.
La mejor forma de medir esa satisfacción por parte del paciente es la utilización de encuestas. Las encuestas de satisfacción realizadas por los profesionales sanitarios a los pacientes en relación a la toma de diferentes medicamentos, permite conocer que es lo que más preocupa al paciente respecto a su tratamiento para poder idear estrategias que permitan mejorar el tratamiento activo actual y considerar dichos aspectos para aplicarlos en el futuro16.
Nuestro estudio ha permitido conocer, mediante la realización del cuestionario TSQM, la satisfacción que el paciente diagnosticado de EM que inicia tratamiento con fampridina tiene respecto de ese medicamento, una vez que ha superado los 14 días iniciales de tratamiento recomendados para continuar con el mismo.
CONCLUSIONES
En nuestro caso, en base a los resultados de efectividad, logrando reducción de T25FW, y satisfacción global de la encuesta se puede concluir que el medicamento utilizado cumple las expectativas de los pacientes, si bien para la obtención de conclusiones definitivas se requieren series mayores que se presentan como World Real Patients.
Conflicto de intereses: Los autores declaran no tener conflictos de intereses.
Bibliografía
1. Oreja-Guevara C, Montalban X, De Andrés C, Casanova-Estruch B, Muñoz-García D, García I, et al. Documento de consenso sobre la espasticidad en pacientes con esclerosis múltiple. Rev Neurol. 2013;54(8):359-373.
2. Tratamiento a largo plazo en la esclerosis múltiple. [monografía en internet]. Madrid: Acción Médica 2008. [citado 12 diciembre 2014]. Disponible en: http://www. monografiasesclerosismultiple.com/visualizador.html?id=004.
3. Files DK, Jausurawong T, Katrajian R, Danoff R. Multiple Sclerosis. Prim Care Clin. 2015;42(2):159-75.
4. Qué es la Esclerosis Múltiple. Esclerosis Múltiple España [Internet]. Madrid 2015 [24 junio 2015]. Disponible en: http://www.esclerosismultiple.com/esclerosis_multiple/EM_que.php.
5. Multiple Sclerosis: A Review and Treatment Option Updates.[internet] Alabama Pharmacy Association 2014 [citado 30 agosto 2015]. Disponible en: http:// c.ymcdn.com/ sites/www.aparx.org/resource/resmgr/CEs/CE_Test_MS_Review_and_Treatm.pdf.
6. Guía Oficial para el diagnóstico y tratamiento de la esclerósis multiple. [Monografía en internet]. Barcelona: Grupo de Enfermedades Desmielinizantes de la Sociedad Española de Neurología; 2007 [citado 12 diciembre 2014]. Disponible en: http://docplayer.es/ 6177509-Prous-science-s-a-2007-provenza-388-08025-barcelona-espana.html.
7. Tratamiento Sintomático en Esclerosis Múltiple. [Monografía en internet]. Madrid: Acción Médica 2009 [citado 12 diciembre 2014]. Disponible en: http:// www.monografiasesclerosismultiple.com/visualizador.html?id=007.
8. Pozzilli C. Overview of MS Spasticity. European Neurology;(suppl 1):1-3.
9. Vivancos-Matellano F, Pascual-Pascual SI, Nardi-Vilardaga J, Miquel-Rodriguez F, de Miguel-León I, Martínez-Garre MC, et al. Guía del tratamiento integral de la espasticidad. Rev Neurol. 2007;45(6):365-375.
10. Ficha técnica Sativex®. [consultado 5 de agosto 2016]. Disponible en: https://www.aemps.gob.es/cima/ dochtml /ft/72544/FichaTecnica_72544.html.
11. Ramió-Torrentá L, Álvarez-Cermeño JC, Arroyo R, Casanova-Estruch B, Fernández O, García-Merino JA, et al. Guía de tratamiento del deterioro de la marcha con fampridina de liberación prolongada (Fampyra®) en pacientes con esclerosis múltiple. Neurología [internet]. 2015 [citado 13 diciembre 2015]; Disponible en: http://www.sciencedirect.com/science/article/pii/S0213485315002698.
12. Ficha técnica Fampyra®. [consultado 3 diciembre 2015]. Disponible en: http://www.ema.europa.eu/docs/es_ ES/ document_library/EPARProduct_Information/human/002097/WC500109956.pdf.
13. Rabadi MH, Kreymborg K, Vicent AS. Sustained-Release Fampridine (4-Aminopyridine) in Multiple Sclerosis: Efficacy and Impact on Motor Function. Drugs R D. (2013);13(3):175-181.
14. Goodman AD, Brown TR, Krupp LB, Schapiro RT, Schwid SR, Cohen R, et al. Sustained-release oral fampridine in multiple sclerosis: a randomised, double-blind, controlled trial. Lancet. 2009;373(9665):732-738.
15. Goodman AD, Brown TR, Edwards KR, Krupp LB, Schapiro RT, Cohen R, et al. A phase 3 trial of extended reléase oral dalfampridine in multiple sclerosis. ANN Neurol. 2010;68(4):494-502.
16. Cameron MH, Fitzpatrick M, Overs S, Murchison C, Manning J, Whitham R. Dalfampridine improves walking speed, walking endurance, and community participation in veterans with multiple sclerosis: a longitudinal cohort study. Multiple Sclerosis Journal. 2014;20(6):733-738.
17. Villar López J, Lizán Tudela L Soto Álvarez J, Peiró Moreno S. La satisfacción con el tratamiento. Atención Primaria. 2009;41(11):637-645.
____
Descargar PDF:Fampridina, esclerosis múltiple, satisfacción del paciente
