Díez López I1, Sarasua Miranda A2, Lorente Blázquez I2, Mínguez AC3, Martínez Martínez C3
1 Unidad de Endocrino Infantil. Servicio de Pediatría. Hospital Universitario Araba. Vitoria. UPV-EHU. Facultad de Medicina. Vitoria (España)
2 Unidad de Endocrino Infantil. Servicio de Pediatría. Hospital Universitario Araba. Vitoria (España)
3 Servicio de Farmacia. Hospital Universitario Araba. Vitoria (España)
Fecha de recepción: 17/04/2018 – Fecha de aceptación: 16/06/2018
Correspondencia: Ignacio Díez López w Hospital Universitario Araba (Servicio de Pediatría) w C/Jose Atxotegi, s/n w 01009 Vitoria-Gasteiz, Álava (España)
ignacio.diezlopez@osakidetza.eus
____
Resumen
Objetivos: Determinar el uso real de la hormona de crecimiento (GH) en la población pediátrica de un centro de referencia de endocrinología pediátrica en la región/Araba (España): dosis utilizada y costes asociados por presentación de GH aprobada. Esto permitiría establecer mejoras estratégicas para optimizar el tratamiento (adherencia/efectividad).
Métodos: Estudio observacional, retrospectivo, en la población pediátrica de un centro de nivel IIb con GH durante 2012. Se calculó la diferencia anual por paciente entre la dosis de GH recibida (mg recogidos) y la dosis prescrita (mg pautados) y los costes asociados de forma global y para cada una de las presentaciones (monodosis [JM], viales multidosis [VM] y dispositivos electrónicos [DE]). Adicionalmente, se hizo una estimación de los mg recogidos y el coste que supondría utilizar exclusivamente cada una de las presentaciones.
Resultados: El 57% de los pacientes recogió menos mg de los pautados (12% incumplidores); dispensándose una dosis 1,3% inferior de la prescrita. Los dispositivos más empleados fueron los JM. La única presentación que mostró desperdicio de GH fue la de VM, con las mayores diferencias entre dosis recibida vs. prescrita. En la estimación para cada presentación, los JM y DE supondrían un uso más aproximado al prescrito, con unos costes no mucho más elevados a los de la mayoría de los VM.
Conclusiones: El uso mayoritario de JM evita desperdicio de GH. Junto con los DE son los dispositivos que muestran menor desviación del tratamiento de GH indicado (mayor adherencia). Su uso implicaría mejores resultados en la salud, con unos costes no muy superiores frente a los VM.
Palabras clave: Hormona de crecimiento, dispositivos de administración de fármacos, adherencia, análisis de costes.
____
Introducción
El déficit de la hormona de crecimiento (GHD), constituye una serie de anomalías causadas por la ausencia o cantidades insuficientes de hormona de crecimiento (GH). El diagnóstico del GHD infantil viene dificultado por la falta de clínica, justificando la falta de precisión en los datos de prevalencia1 (rango 1/4.0002-1/30.000 niños3).
El GHD puede tener un impacto en la vida del individuo desde la infancia hasta la edad adulta (talla, repercusiones metabólicas, efectos psicológicos…)1,4. Resulta por lo tanto fundamental su diagnóstico temprano para su adecuado tratamiento (reemplazo hormonal con GH recombinante humana).
Las indicaciones de la GH actualmente aprobadas en España (uso hospitalario) son: DGH clásico, síndrome de Turner (ST), insuficiencia renal crónica en niños en periodo prepuberal, síndrome de Prader-Willi, paciente pequeño para la edad gestacional (PEG) y deficiencia de crecimiento por alteración del gen SHOX1.
El reemplazo hormonal con GH es un tratamiento a largo plazo, que en pacientes pediátricos presenta una falta de adherencia (administración de forma diferente a lo prescrito por el médico) estimada entre el 5% y 82%5. Esta falta de adherencia, puede explicarse entre otras razones por la duración del tratamiento y aspectos relacionados con los dispositivos de administración5. Las formulaciones de GH comercializadas para inyección subcutánea (SC) diaria son: jeringas monodosis (JM), viales multidosis precargados (VM) y sistemas con dispositivos electrónicos (DE) de autoinyección.
La no adherencia al tratamiento de reemplazo conlleva incrementos en el coste sanitario y peores resultados (efectividad clínica)5-7; reflejándose en un empeoramiento del coste-efectividad del tratamiento y en la calidad de vida del paciente. Por ese motivo es crucial fomentar y controlar la adherencia8. Para dicho control pueden emplearse métodos indirectos, como los niveles de factor de crecimiento insulinoide tipo 1 (IGF-1)8; o directos, como el uso de DE cuya tecnología permite un control más preciso que otras técnicas8,9. Los DE son los dispositivos que menos cantidad de GH desperdician respecto a los otros tipos de dispositivos10 y más adherencia presentan7,11. Entre los dispositivos manuales, los que menos gastos llevan asociados son aquellos más rápidos de utilizar12.
El objetivo principal de este estudio es determinar el uso real de la GH en la población pediátrica y realizar un análisis comparativo de costes y pérdida de producto entre las diferentes presentaciones aprobadas en España. Como objetivo secundario se pretende observar diferencias de efectividad en el tratamiento con GH, en base a las diferencias detectadas según presentación entre las dosis prescritas y las recibidas por los pacientes. Los resultados permitirán establecer/fomentar mejoras estratégicas a seguir para aumentar la adherencia y alcanzar mayor efectividad.
MÉTODO
Estudio retrospectivo, observacional, en el que se realizó un análisis comparativo de dosis y costes de la GH prescrita (endocrino) y la recogida en farmacia (pacientes). El estudio fue autorizado por el comité ético de investigaciones clínicas del Hospital Universitario de Álava (HUA) (12/2014).
La población del estudio estaba constituida por todos los pacientes pediátricos tratados en la unidad de Endocrinología Infantil de Pediatría del centro IIb de referencia de Endocrinología Pediátrica de la región/Áraba durante el 2012. Debían tener datos de todas las dispensaciones mensuales de GH.
Los datos se obtuvieron de forma retrospectiva de las historias clínicas y del programa de dispensación de farmacia, respetando siempre la confidencialidad acorde con la Ley Orgánica de Protección de Datos (15/1999, 13-diciembre).
Se recogieron los datos anuales sobre la dosis de GH prescrita (mg pautados) y la recibida (mg recogidos) por paciente. Con ellos se calculó el precio prescrito y el real gastado con cada una de las presentaciones de GH (JM [Genotonorm® MINIQUICK], VM [Humatrope®, Norditropin®. Zomacton®]) y DE [Saizen®; con automatismo que permite ajustar ≤10% la dosis prescrita para no desperdiciar producto].
Otras variables recogidas fueron: sexo, edad al inicio del estudio (01-enero-2012), indicación (déficit clásico de GH, PEG, trastorno de crecimiento asociado a ST, disfunción-inactividad biológica de la GH y otros), niveles de IGF-1 en suero (ng/ml) y velocidad de crecimiento como medida de seguimiento y efectividad del tratamiento con GH. Los niveles de IGF-1 se determinaron mediante un método inmunométrico quimioluminiscente (IMMULITE 2000 IGF-1. PIL2KGF-17, 2009-10-06).
Se calculó la diferencia anual por paciente entre la dosis de GH recibida (mg recogidos) y la prescrita (mg pautados) de forma global y para cada una de las presentaciones farmacéuticas. También se calculó el porcentaje de GH recibida vs. prescrita (positivo si se consumía de más; negativo si se consumía de menos). Se definió incumplimiento como la pérdida de ≥15% de las dosis (≥1 inyección/semana).
Con los datos de dosis obtenidos se obtuvo el precio anual real gastado vs. prescrito utilizando el coste farmacológico (PVL 2012) de cada una de las presentaciones en el momento del estudio.
Finalmente, se estimó el impacto económico que supondría la administración del total de mg pautados utilizando exclusivamente cada una de las presentaciones de GH. Para ello se calculó el coste teniendo en cuenta la variación de mg calculada previamente con cada dispositivo.
Para el análisis estadístico de los resultados se utilizó el programa SPSS 19.0 IBM. Se realizó un análisis descriptivo para determinar los valores de media, mediana y desviación típica estándar (DE) de la edad, y media y mediana de la diferencia de dosis total y del porcentaje de GH recibida vs. prescrita. Se usó el test (X2) para muestras apareadas (n<30), considerándose asociación estadística con niveles de significación superiores al 95% (p<0,05). Para estimar las diferencias entre las distintas presentaciones entre mg GH pautados y recogidos, se realizó la prueba ANOVA.
RESULTADOS
Se incluyeron 88 pacientes; 2 fueron descartados por falta de datos. Entre los 86 pacientes analizados, la edad media fue de 10,9 años; desviación estandar 3,0 (mediana=11,2 años; rango 4,9-17,0 años). El 65% de la población eran púberes (B2 o G2 en la escala Tanner) y 50% eran varones.
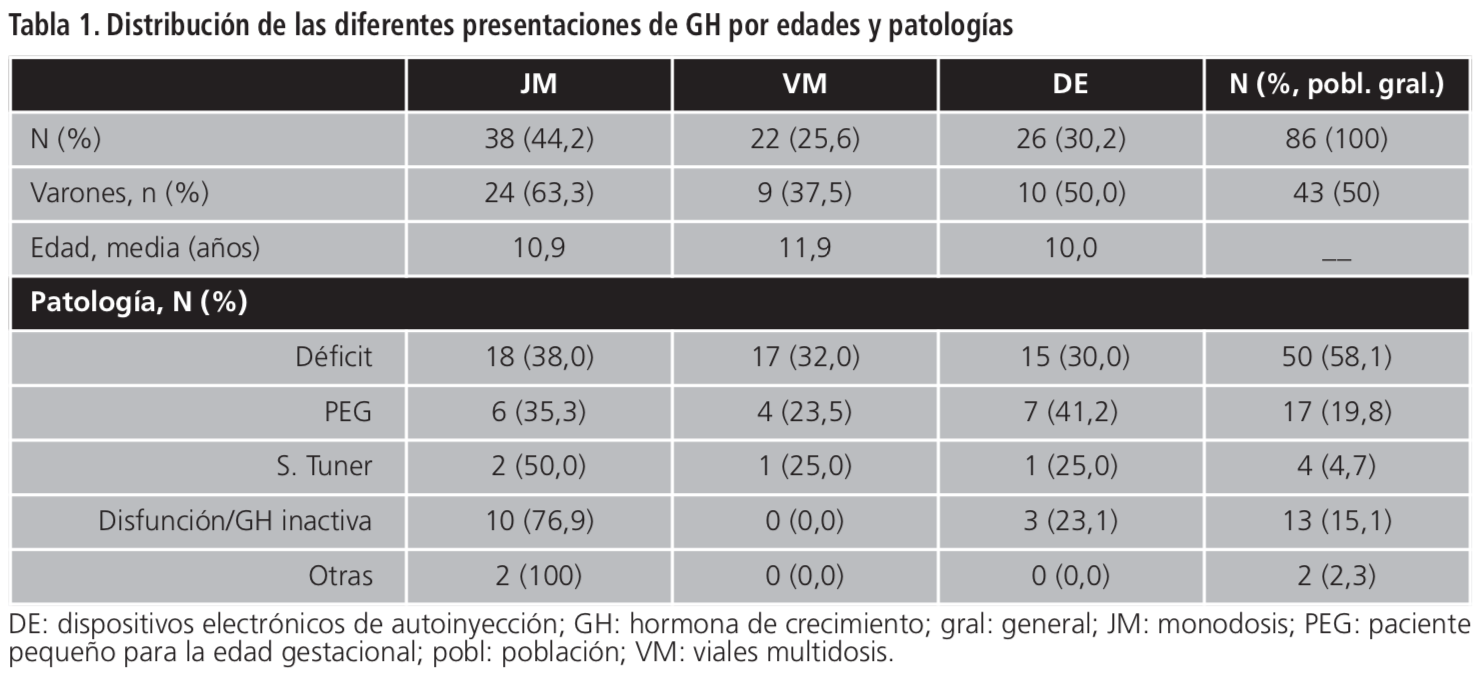
La indicación de GH más frecuente fue déficit clásico de GH (58,1% pacientes), seguida de PEG, disfunción-inactividad biológica de la GH y ST (4,6% pacientes) (Tabla 1). Y la presentación más utilizada de GH fue la de monodosis (JM, Genotonorm®, 44,2%) en todas las patologías, excepto en PEG, con mayor uso del DE (Tabla 1). Entre las presentaciones de VM disponibles, la más empleada fue Humatrope® (n=13), seguido de Norditropin® (n=6) y Zomacton® (n=3). Los pacientes que utilizaron VM fueron los de mayor edad; los de menor edad utilizaron DE (Tabla 1).
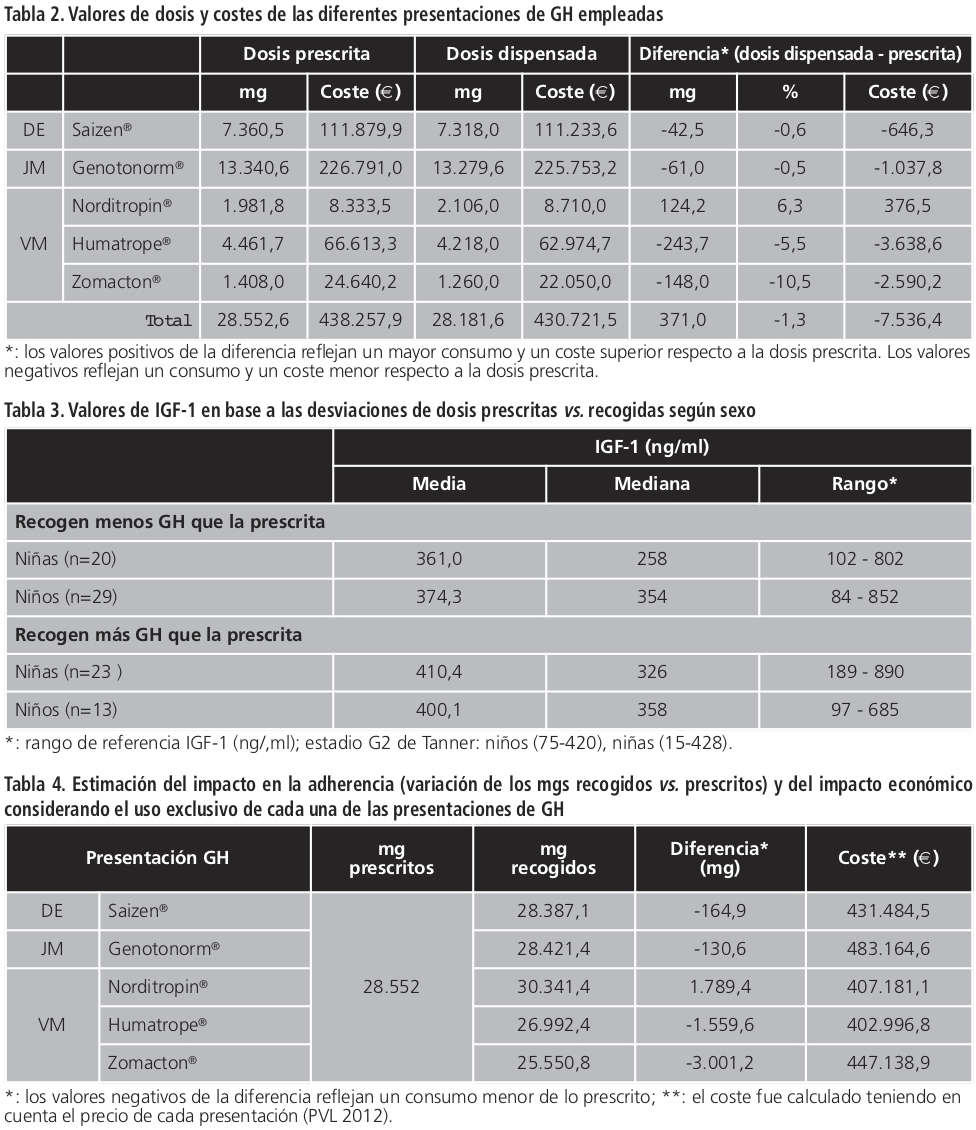
De los 28.552,7 mg prescritos, los pacientes recogieron 28.181,6 mg; 371 mg (1,3%) menos. La dosis global media de GH prescrita fue 332,0 mg (rango 0-998 mg), y la recogida en farmacia fue 327,7 mg (rango, 36-960 mg).
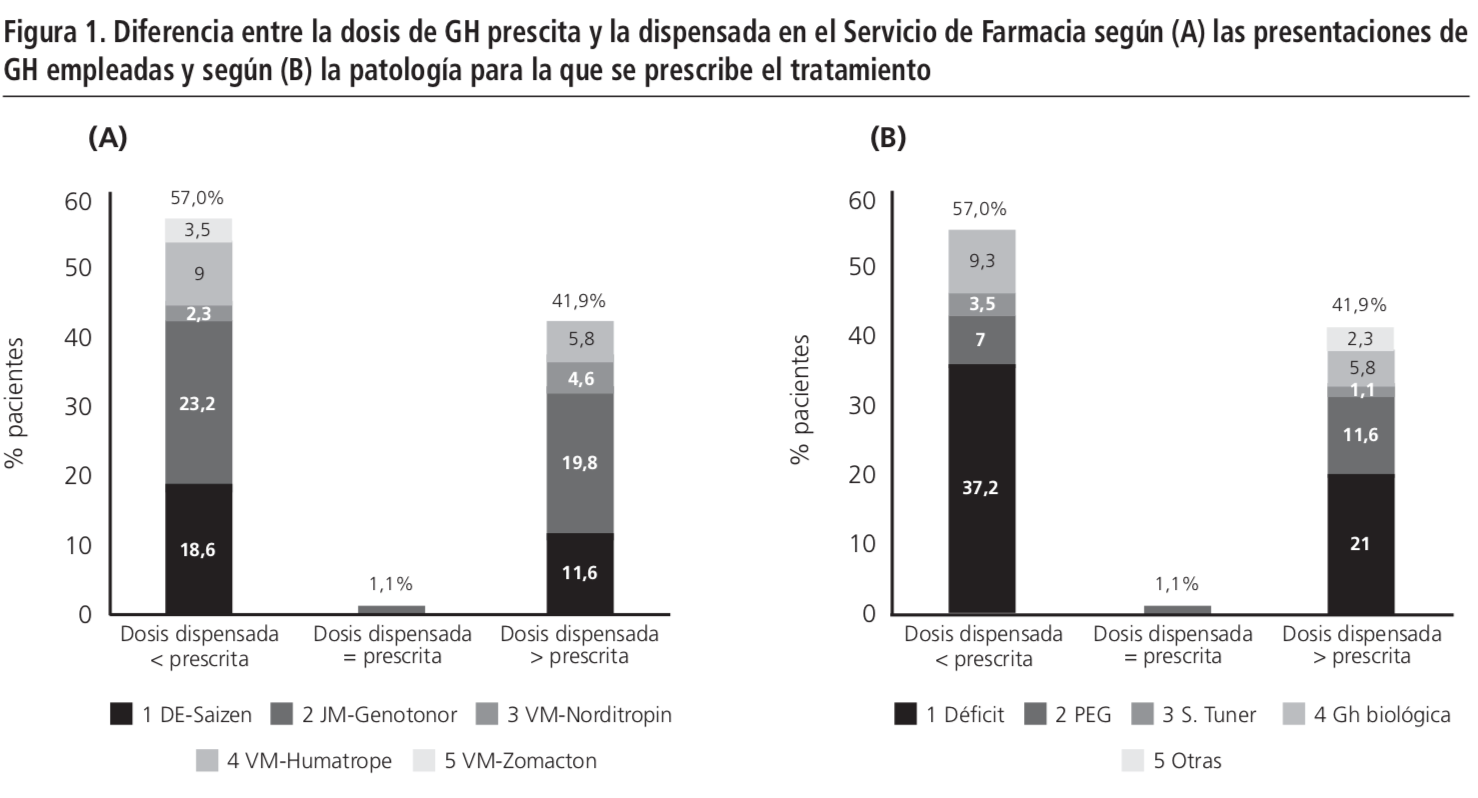
Analizando la diferencia por paciente entre dosis recogida y prescita, se observó que únicamente un paciente (1,1%) recogió los mg prescritos (Figura 1); 36 (41,9%) pacientes recogieron más mg (media 27,0 mg; mediana, 12,9 mg; rango 0,9-117,0 mg), y 49 (57,0%) pacientes recogieron menos mg (media 27,4 mg; mediana, 11,8 mg; rango -158,2; -0,4 mg). Diez (11,3%) pacientes fueron considerados incumplidores, con una pérdida >15% de la dosis. Mediante el software específico del DE se comprobó una adherencia media del 97,5% (mediana 96,8%).
El valor medio de IGF-1 en sangre fue mayor en los pacientes que recogieron más GH de la prescrita frente a los que recogieron menos (Tabla 3), estando aun así dentro de los rangos de normalidad. El análisis comparativo entre los diferentes dispositivos no mostró diferencias significativas en velocidad de crecimiento (p=0,39), sexo (p=0,21) y dosis pautada (p=0,52). Sí que se observó una diferencia significativa en las dosis recogidas (p=0,01) a favor de los VM vs. JM y DE.
La presentación de GH con la que los mg prescritos se aproximan más a los recogidos es la de JM (Genotonorm®), seguido muy de cerca por el DE (Tabla 2). El VM, Zomacton® es el que muestra mayor diferencia. Independientemente de recoger más o menos dosis de la prescrita, la desviación fue más frecuente en los pacientes que utilizaron JM (Figura 1A).
Analizando según indicación, el tipo de patología no mostró variaciones en el cumplimiento; se observó un porcentaje superior de pacientes que recogieron menos mg de GH de los prescritos en todos los casos, excepto en PEG, en el que fue superior el porcentaje de pacientes que recogieron más mg de los prescritos (Figura 1B).
Respecto el aspecto económico, la diferencia entre los mg totales prescritos (coste 438.258€), y los dispensados (coste 430.721€), resultó en 7.536€ (1,3% menos) (Tabla 2). La presentación cuyo uso exclusivo conllevaría más gastos es la del JM, seguido de VM (Zomacton®) y DE (Tabla 4). El precio inferior del VM (Norditropin®), correspondiente al de 2012, conllevaría que fuera una de las presentaciones con menos gastos, pese a ser la única presentación que implicaría una dispensación de más mg de GH de los prescritos.
DISCUSIÓN
Los resultados de este estudio observacional retrospectivo reflejan el uso real de la medicación por los pacientes pediátricos tratados con GH durante el año 2012 en un hospital de Vitoria.
La adherencia al tratamiento, especialmente en los de larga duración, es un factor fundamental para asegurar su efectividad13. En el caso del tratamiento con GH, su larga duración y las inyecciones diarias, dificultan la adherencia; conllevando respuestas sub-óptimas (reducción del crecimiento lineal estimado)8,14,15. En la población de nuestro estudio (n=86), sólo un paciente recogió la dosis de GH prescrita y aproximadamente la mitad (57%) recogió menos, con 12% de incumplidores. Nuestros resultados difieren bastante de otro estudio en un centro español (Barcelona), donde 16% de los pacientes 16 recogieron menos dosis de la prescrita y 6,3% fueron incumplidores (recogieron ≤92% de la dosis prescrita)16. La definición de incumplimiento suele basarse en las dosis perdidas, y varía mucho en los diferentes estudios publicados5. Comparando el incumplimiento obtenido en nuestro estudio (12%) con el de otros (mismo criterio: pérdida de ≥1 dosis/semana), detectamos diferencias: Postlethwite et al. 1998 (6-9%), Kapoor et al. 2008 (>1 dosis/semana, 39%) y Cutfield et al., 2011 (34%)5. Estas diferencias son menores si comparamos estudios con otros criterios de incumplimiento (pérdida de >3 dosis/mes): Stanhope et al. 1993 (10%) y Desrosiers et al. 2005 (15-24%)5. Estas diferencias concuerdan con el alto rango de falta de adherencia descrito para el tratamiento con GH, 5%-82%17.
El tratamiento con GH induce cambios en IGF-115, por ese motivo se ha propuesto como marcador de adherencia8,18, para evitar sobredosis y determinar ajustes de dosis5. Sin embargo, aún hacen falta estudios que comparen los niveles de IGF-1 en pacientes adherentes y no adherentes15. Los niños que recogen más GH de la prescrita podrían ser más adherentes al tratamiento, hecho que podría correlacionarse con los niveles de IGF-1 observados, algo mayores que los de los que recogen menos. Sin embargo, esta diferencia no resultó significativa y los valores de ambos grupos se mantuvieron dentro del rango de normalidad. Dicha variación podría explicarse por la falta de adherencia y justificaría una falta de efectividad del tratamiento, aunque el único caso donde se pudo comprobar la adherencia real fue en el grupo de DE, donde además se demostró una menor pérdida de producto o mejor relación entre prescrito y recogido.
El uso de los diferentes dispositivos de administración de GH no está influenciado por el precio; se determina considerando la preferencia de los pacientes, la facilidad y el número de pasos requeridos para su uso19. Hasta donde nuestro conocimiento alcanza, no se ha descrito que la elección del dispositivo a emplear esté influenciada por la patología asociada al déficit de GH. En nuestro estudio, las JM fueron las más empleadas en todas las patologías, excepto en la PEG, con mayor uso de DE.
Las características diferenciales de los dispositivos pueden conllevar falta de adherencia, con repercusión negativa en la efectividad, e implicar costes sanitarios. La GH es un fármaco biológico, con coste elevado19. El desperdicio de medicación20 y el aumento de la dosis para obtener la respuesta esperada suponen un impacto económico negativo, pero también otras intervenciones relacionadas con la no adherencia como: búsqueda de nuevos diagnósticos, hospitalizaciones…5. Por todo ello es muy importante monitorizar la adherencia; entre los métodos utilizados se encuentran la comunicación con el paciente (consulta, diarios…) y el recuento de viales. El uso de nuevas tecnologías incorporadas a los DE, que recogen y descargan en una base de datos las dosis administradas y el tiempo de la administración, permite un control más fiable21,22.
La mayor simplicidad de los dispositivos listos para usar (JM, Genotonorm®), vs. aquellos que implican reconstitución (VM) conlleva menos pasos y tiempo para su preparación y consigue menos errores19. Estas características, además de favorecer la adherencia, pueden justificar que las JM (Genotonorm®) hayan resultado el dispositivo más empleado en nuestro estudio, con las menores desviaciones de dosis administradas frente a las dosis prescritas (-0,6%). Al ser viales monodosis, solo los olvidos justifican la diferencia observada.
Las mayores variaciones observadas fueron con los VM (Norditropin®, 6,3%; Humatrope®, -5,5% y Zomacton®, -10,5%). La desviación positiva (más mg dispensados vs. prescritos) puede explicarse por la decisión de los progenitores de desechar la cantidad final cuando no alcanza una dosis completa, y empezar una pluma nueva, en lugar de pinchar dos veces a su hijo; esto conlleva malgasto. La población que utilizaba los VM resultó la de mayor edad y aunque se ha descrito que la adherencia no está relacionada con la edad14, las desviaciones negativas podrían justificarse con olvidos, y también por el mayor número de omisiones detectadas en la edad adolescente5.
En el caso de los DE (Saizen®), la adherencia observada (96,8%) fue mayor que la publicada para otros dispositivos8, y en concondarcia con la descrita previamente en España (96,7%23, 98,8%24 y 99,4%25). Sin embargo no era objetivo del presente trabajo estudiar dicho efecto. La diferencia en los mg administrados vs. prescritos fue pequeña, -0,6%, justificada por el automatismo que evita que sobre medicación en el cartucho. También han de considerarse los olvidos.
La mejora estimada de la adherencia con los DE en España (20%) y el ahorro en desperdicio de GH, supondría un ahorro entre el 22-27% del coste de la GH prescrita1.
El malgasto de GH supone hasta un 15% de los gastos relacionados con el tratamiento22. En España, el coste del desperdicio debido a los dispositivos de administración se estima entre el 2,1-7,5%1. Estos valores difieren de los resultados de nuestro estudio en el que, de forma global, no se observó desperdicio sino que se dispensó 1,3% menos de lo prescrito justificándose posiblemente por olvidos de dosis. Únicamente se observó mayor gasto (mg y euros) frente a la dosis prescrita con el VM Norditropin®. Esto refleja que aunque el precio por mg de producto sea más caro en los dispositivos JM y DE, el que eviten pérdida de producto, podría resultar en un ahorro económico y una mayor efectividad del tratamiento.
Al estimar la situación que supondría emplear únicamente cada uno de los dispositivos (Tabla 4), el gasto global en mg resulta más llamativo. Observamos que los dispositivos con menor impacto en la adherencia (variación mg dispensados vs. prescritos) serían las JM y los DE. Este resultado queda justificado porque con las JM no se pierde nada, si no se administra no se recoge de farmacia, y porque con el automatismo del DE se desperdicia menos medicación. Entre los VM, las variaciones serían muy elevadas; las negativas, implicarían una reducción de la efectividad, y las positivas (VM, Norditropín®), supondría un desperdicio de dosis elevado o, en caso de administrarse, posibles efectos adversos (cefalea, problemas visuales, náuseas y vómitos, edema periférico, hipotiroidismo…)18.
En cuanto al impacto económico observado en nuestro estudio, el menor precio de la presentación que mostró desperdicio de GH hace que, de forma general, se gaste menos de lo estimado. Sin embargo, este resultado es circunstancial ya que en cada comunidad autónoma el precio puede variar. Por ese motivo no se debe tener en cuenta el gasto económico sino en el gasto en mg. El precio referencia del producto (€/mg) puede inclinar la balanza a favor de una fórmula u otra. La GH está fuertemente regulada, bajo un régimen de concurso técnico en la mayoría de las comunidades autónomas. Los últimos concursos, inclusive en el País Vasco (2014; 2017) y el ajuste de precio/mg de casi todas las presentaciones en una horquilla muy estrecha (rango 12,50-13 €/mg), conlleva que aquellas con mayor adherencia y menor perdida de producto (mg dispensados vs. gastados) (Saizen® y Genotonorm®) puedieran suponer una diferencia significativa de ahorro en el coste farmacéutico a medio plazo. Nuestros resultados podrían permitir, referente a la gestión económica, una planificación sanitaria del gasto farmacéutico (GH).
Las conclusiones de nuestro estudio in vivo son muy semejantes a las del estudio in silico del Informe Público de Evaluación de Tecnologías Sanitarias IPE 2013/701, en el que se recoge cómo la formula galénica puede influir en la adherencia al tratamiento y en el posible gasto de fármaco por pérdidas de dosis.
Las posibles limitaciones del estudio incluyen su carácter retrospectivo, el periodo analizado de un año y el haberse realizado en un único centro de Álava lo que conlleva además una muestra reducida de pacientes (n=88). Sin embargo, la escasez de datos sobre evaluaciones económicas en España, aportan valor a nuestros resultados.
Conclusión
Nuestros resultados muestran el uso mayoritario de los dispositivos JM. Los valores analizados muestran una mayor variación entre la dosis de GH recogida vs. dispensada con los dispositivos VM frente a los JM y DE, demostrando pérdidas en el mecanismo de dispensación. La estimación económica con cada uno de los dispositivos muestra un coste similar con JM y DE, no mucho superior al que supondría el uso de VM. Sin embargo, la efectividad saldría mucho más favorecida con JM y DE. Disponer de datos sobre qué formulación conlleva mayor adherencia y menor pérdida de dosis en vida real, supone un revulsivo en la práctica clínica diaria y en la gestión sanitaria.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
BIBLIOGRAFÍA
1. Saz-Parkinson Z, Granados MS, Almendro Motos N, Amate Blanco JM. Adherencia al tratamiento con Hormona de Crecimiento Recombinante en niños deficitarios: Control terapéutico e impacto económico –EPÍTOME Informe IPE 2013/70. Madrid: Agencia de Evaluación de Tecnologías Sanitarias (AETS) del Instituto de Salud Carlos III; 2013.
2. Murray PG, Dattani MT, Clayton PE. Controversies in the diagnosis and management of growth hormone deficiency in childhood and adolescence. Archives of disease in childhood. 2016;101(1):96-100.
3. Thomas M, Massa G, Craen M, de Zegher F, Bourguignon JP, Heinrichs C, et al. Prevalence and demographic features of childhood growth hormone deficiency in Belgium during the period 1986-2001. Eur J Endocrinol. 2004; 151(1):67-72.
4. Ahmid M, Perry CG, Ahmed SF, Shaikh MG. Growth hormone deficiency during young adulthood and the benefits of growth hormone replacement. Endocr Connect. 2016;5(3):R1-R11.
5. Fisher BG, Acerini CL. Understanding the growth hormone therapy adherence paradigm: a systematic review. Horm Res Paediatr. 2013;79(4):189-196.
6. Rosenfeld RG, Bakker B. Compliance and persistence in pediatric and adult patients receiving growth hormone therapy. Endocr Pract. 2008;14(2):143-154.
7. Saz-Parkinson Z, Granados M, Bouza C, Poveda-Andrés JA, Amate JM. Self-administration of Recombinant Human Growth Hormone with an Electronic Device: Clinical, Economic and Management Benefits of Objective Adherence Monitoring. Journal of Health Economics and Outcomes Research. 2014; 1(3):296-307.
8. Acerini CL, Wac K, Bang P, Lehwalder D. Optimizing Patient Management and Adherence for Children Receiving Growth Hormone. Frontiers in endocrinology. 2017;8:313.
9. van Heuckelum M, van den Ende CHM, Houterman AEJ, Heemskerk CPM, van Dulmen S, van den Bemt BJF. The effect of electronic monitoring feedback on medication adherence and clinical outcomes: A systematic review. PloS one. 2017;12(10):e0185453.
10. Mas Comas A, López Ramos MG, Villaronga FLaqué M, Murciano Cabeza A, Díaz Cerezo S, Farré Riba R. Análisis comparativo de costes entre distintas presentaciones de hormona de crecimiento. Atención farmacéutica. 2012; 14(5):329-336.
11. Locklear J, Edwards N, Phillips AL. Evaluation of Potential Waste Of Growth Hormone Across Available Growth Hormone Pen Devices And An Electronic Growth Hormone Delivery Device. Value in Health. 2014;17(7):A338.
12. Nickman NA, Haak SW, Kim J. Cost minimization analysis of different growth hormone pen devices based on time-and-motion simulations. BMC nursing. 2010;9:6.
13. Brown MT, Bussell JK. Medication adherence: WHO cares? Mayo Clinic proceedings. 2011;86(4):304-314.
14. Cutfield WS, Derraik JG, Gunn AJ, Reid K, Delany T, Robinson E, et al. Non-compliance with growth hormone treatment in children is common and impairs linear growth. PloS one. 2011;6(1):e16223.
15. Loche S, Salerno M, Garofalo P, Cardinale GM, Licenziati MR, Citro G, et al. Adherence in children with growth hormone deficiency treated with r-hGH and the easypod device. J Endocrinol Invest. 2016;39(12):1419-1424.
16. Mas-Comas A, López-Ramos MG, Villaronga-Flaqué M, Murciano-Cabeza A, Díaz-Cerezo S, Farré-Riba R. Análisis comparativo de costes entre las distintas presentaciones de hormona de crecimiento: jeringas monodosis vs viales multidosis. Rev Esp Endocrinol Pediatr. 2011;P1/d2-3-015(2 (Suppl)).
17. Spoudeas HA, Bajaj P, Sommerford N. Maintaining persistence and adherence with subcutaneous growth-hormone therapy in children: comparing jet-delivery and needle-based devices. Patient preference and adherence. 2014; 8:1255-1263.
18. Sayarifard F, Imcheh FB, Badri S, Faghihi T, Qorbani M, Radfar M. Growth Hormone Utilization Review in a Pediatric Primary Care Setting. Journal of research in pharmacy practice. 2017;6(1):40-43.
19. Chapman SR, Fitzpatrick RW, Aladul MI. What drives the prescribing of growth hormone preparations in England? Prices versus patient preferences. BMJ open. 2017;7(4):e013730.
20. West LM, Borg Theuma R, Cordina M. Health locus of control: Its relationship with medication adherence and medication wastage. Research in social & administrative pharmacy: RSAP. 2017.
21. Christiansen JS, Backeljauw PF, Bidlingmaier M, Biller BM, Boguszewski MC, Casanueva FF, et al. Growth Hormone Research Society perspective on the development of long-acting growth hormone preparations. Eur J Endocrinol. 2016; 174(6):C1-8.
22. Rohrer TR, Horikawa R, Kappelgaard AM. Growth hormone delivery devices: current features and potential for enhanced treatment adherence. Expert opinion on drug delivery. 2017;14(11):1253-1264.
23. Bozzola M, Colle M, Halldin-Stenlid M, Larroque S, Zignani M, easypod survey study g. Treatment adherence with the easypod growth hormone electronic auto-injector and patient acceptance: survey results from 824 children and their parents. BMC endocrine disorders. 2011;11:4.
24. Rodríguez-Arnao MD, Rodríguez Sánchez A, Díez López I, Ramírez Fernández J, Bermúdez de la Vega JA, Ballano V, et al. Spanish ECOS Study Analysis: Socioeconomic Data, Adherence and Growth Outcomes with Case Studies.Abstract P1-69. Presented at ESPE 2016; September 10-12; Paris, France.
25. Rodríguez-Arnao MD, Rodríguez Sánchez A, Peláez Muñoz R, Díez López I, Joaquín Ramírez Fernándes J, Bermúdez de la Vega JA, et al. Ecos Study Analysis: Injection Settings and Adherence Data from Spain. Abstract SAT-042 of the Endocrine Society’s 98th Annual Meeting and Expo, April 1-4, 2016 – Boston.
____
