Comet-Bernad M, Uriarte-Pinto M, Galindo-Allueva M, Huarte-Lacunza R, Abad-Sazatornil MR
Servicio de Farmacia. Hospital Universitario Miguel Servet. Zaragoza (España)
Fecha de recepción: 07/06/2018 – Fecha de aceptación: 18/07/2018
Correspondencia
Macarena Comet-Bernad w Hospital Universitario Miguel Servet (Servicio de Farmacia) w Paseo Isabel la Católica, 1-3 w 50009 Zaragoza (España)
mcomet7@gmail.com
____
Resumen
Objetivos: La infección de heridas crónicas es una complicación de elevada prevalencia con una alta morbi-mortalidad asociada. Las bacterias gram-negativas están frecuentemente relacionadas con este tipo de infecciones. La creciente incidencia de cepas multiresistentes o extremadamente resistentes sumado a la gran capacidad de las bacterias gram-negativas para desarrollar resistencias hace que la colistina sea en ocasiones la única opción de tratamiento. La ausencia de antibióticos tópicos para el tratamiento de estas infecciones, llevó a la elaboración de una crema tópica de colistina para satisfacer esta laguna terapéutica en nuestro país.
Métodos: Se llevó a cabo un estudio descriptivo de una serie de casos tratados con crema tópica de colistina al 0,1%. El objetivo del estudio fue evaluar su eficacia en la erradicación de las infecciones de heridas crónicas causadas por bacterias gram-negativas. Otros objetivos incluyeron la evaluación de la seguridad y del tiempo hasta la erradicación de la infección. La crema fue elaborada en el servicio de Farmacia de un hospital de tercer nivel, según las guías de buenas prácticas de elaboración.
Resultados: Diez pacientes con infección de herida crónica debida a bacterias gram-negativas fueron tratadas con la crema de colistina 0,1%. Se observó un 80% de erradicación con una mediana de tiempo hasta la erradicación de 3,5 semanas. Ningún paciente comunicó efectos adversos locales o sistémicos, ni reacciones de hipersensibilidad.
Conclusiones: La crema de colistina parece ser una alternativa eficaz y segura para el tratamiento de las infecciones de heridas crónicas causadas por bacterias gram-negativas.
Palabras clave: Bacterias gram-negativas, infección, heridas, colistina, tópico.
____
Introducción
Se define herida crónica como aquella que no ha cicatrizado en 4-6 semanas. Se estima que aproximadamente un 1-2% de la población en países desarrollados puede llegar a padecerlas a lo largo de su vida1.
La infección de estas heridas es una complicación de elevada prevalencia que, además de dificultar la cicatrización, provoca una elevada morbi-mortalidad1-3, y consecuentemente un coste adicional para los sistemas sanitarios4. Esto explica la importancia del uso racional de antibióticos, así como la creciente preocupación por la aparición de microorganismos resistentes.
Con frecuencia la flora aislada en las heridas crónicas es compleja, polimicrobiana y a menudo cambiante a lo largo del tiempo2,3. Staphylococcus aureus y estafilococos coagulasa-negativos son las bacterias aisladas con mayor frecuencia, sin embargo, especies como Enterococcus faecalis, Pseudomonas aeruginosa, Proteus spp, Escherichia coli o Klebsiella spp son también comunes1-3.
La identificación precoz y determinación de la sensibilidad antibiótica juega por lo tanto un papel muy importante a la hora de seleccionar la terapia más adecuada5.
En los últimos años, el tratamiento de las infecciones por bacilos gram-negativos (BGN) se ha convertido en un reto debido al aumento en la incidencia de aparición de cepas multirresistentes (MDR) y extremadamente resistentes (XDR). Esta circunstancia, junto con la ausencia de nuevos antibióticos frente a este grupo de bacterias, ha favorecido que se incremente el uso de antiguos fármacos como la colistina6.
La administración sistémica de colistina presenta la desventaja de una escasa penetración a algunos tejidos7,8. Es por eso que su uso en el tratamiento de la infección de heridas podría requerir aumentar la dosis con el objetivo de alcanzar concentraciones terapéuticas en el foco de la infección, aumentando el riesgo de toxicidad.
Con el objetivo de optimizar el tratamiento de estas heridas se plantea el uso tópico de crema de colistina, elaborada como fórmula magistral desde los Servicios de Farmacia, debido a la ausencia de medicamentos tópicos comercializados con este principio activo en nuestro medio.
En la actualidad es escasa la evidencia disponible respecto al uso de la colistina tópica para el tratamiento de estas infecciones, por lo que se considera necesaria la aportación de los resultados obtenidos en su uso en la práctica clínica.
MATERIAL Y MÉTODOS
Se trata de un estudio descriptivo retrospectivo de una serie de casos tratados con crema de colistina 0,1% en el periodo comprendido entre julio de 2014 y septiembre de 2015.
Se registraron de forma anónima datos demográficos, tipo y tiempo de evolución de la herida, microorganismo aislado, duración del tratamiento, erradicación del microorganismo, tiempo hasta la erradicación y observaciones clínicas particulares para cada paciente.
El objetivo principal del estudio fue describir la eficacia del empleo de crema tópica de colistina 0,1% para el tratamiento de heridas infectadas por bacilos y cocobacilos gram-negativos. Los objetivos secundarios fueron la evaluación de la seguridad del tratamiento con colistina tópica, así como la evaluación del tiempo hasta la erradicación.
La variable principal del estudio fue la erradicación del microorganismo. Las variables secundarias fueron la presencia o no de efectos adversos tanto locales como sistémicos y el tiempo hasta la erradicación. Se definió erradicación como la negativización de los cultivos microbiológicos de la herida.
Preparación de la fórmula magistral
La elaboración de la fórmula magistral se realizó en el Servicio de Farmacia según lo descrito en la bibliografía9,10 y siguiendo las normas del Formulario Nacional y la Guía de buenas prácticas de preparación de medicamentos en Servicios de Farmacia Hospitalaria11,12.
La preparación de la crema de colistina al 0,1% se realizó a partir de los viales de colistimetato de sodio G.E.S 1MUI y de base Beeler y agua estéril como excipientes. Cada vial de colistimetato de sodio fue reconstituido con 2 ml de agua estéril. Con el objetivo de hacer la base Beeler más fluida, bajo agitación, se añadió lentamente agua estéril en proporción 1:1. Una vez la mezcla de base Beeler y el agua se emulsificaron correctamente se añadió la colistina poco a poco hasta asegurar su completa homogeneidad. Finalmente, se envasó protegida de la luz debido a la fotosensibilidad del colistimetato de sodio y se etiquetó dándole un mes de estabilidad según la bibliografía9,11.
RESULTADOS
Se incluyeron un total de 10 pacientes, 50% mujeres. La mediana de edad fue de 65 años (IC 95%: 35-78). Respecto a la etiología de la herida, 4 pacientes (40%) presentaban úlcera por presión, 2 (20%) herida quirúrgica, 2 (20%) eran grandes quemados, presentando los 2 restantes lesiones necróticas de diferente origen (calcifilaxia y síndrome de Steven-Johnson).
La mediana del tiempo de evolución de las heridas fue de 3 meses (IC 95%: 1-84).
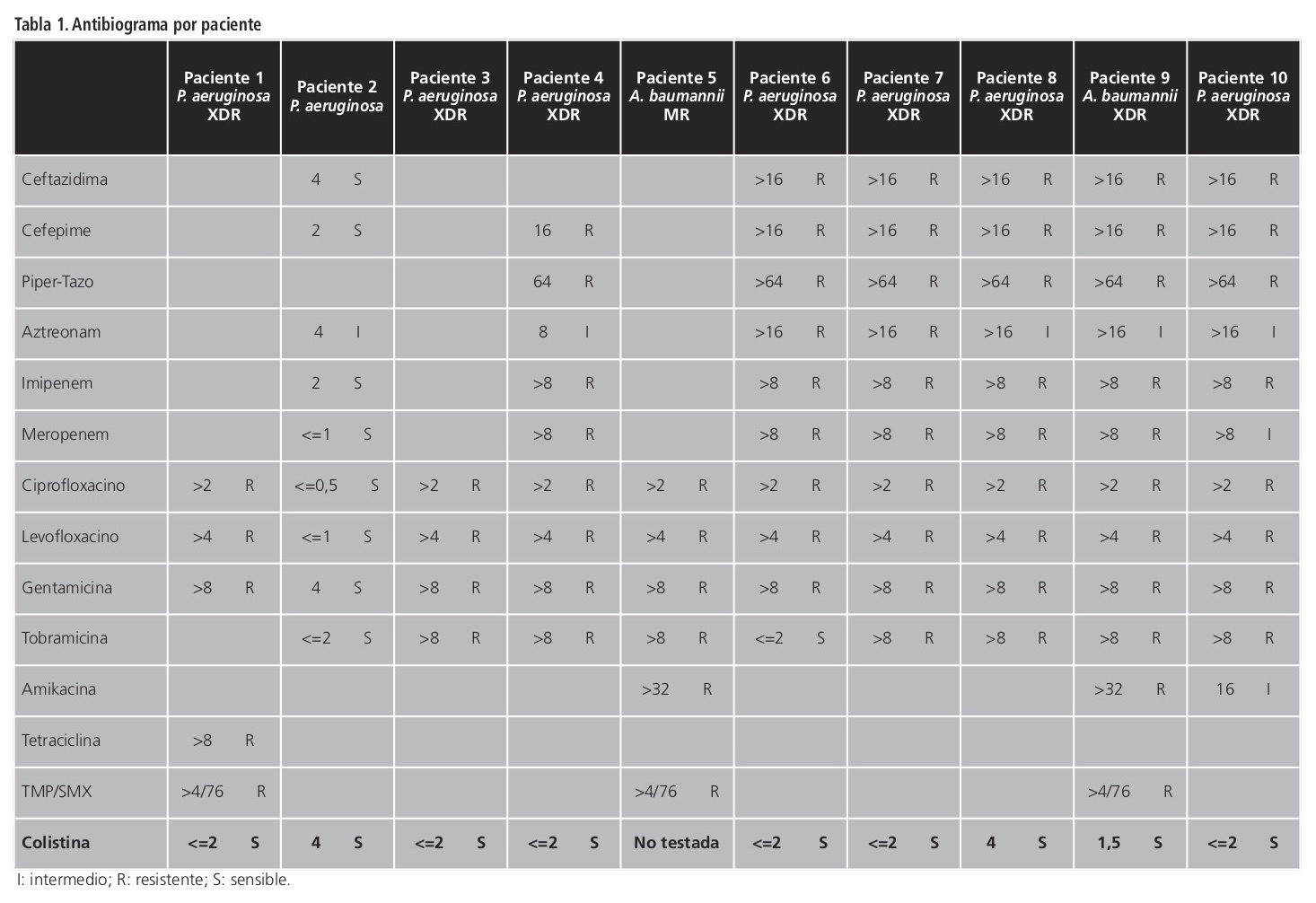
Como se muestra en la Tabla 1, en el 80% de los casos (8/10) se aisló P. aeruginosa, siendo cepas extremadamente resistentes (P. aeruginosa XDR) en siete de ellos. Acinetobacter baumannii fue el microorganismo aislado en los dos casos restantes, una de las cepas extremadamente resistente y la otra pan-resistente (A. baumannii XDR y PDR, respectivamente).
En relación al objetivo primario, se observó la erradicación del microorganismo en el 80% de los casos (8/10). La mediana de duración del tratamiento fue de 3,5 semanas (IC 95%: 0,5-10,1).
De los dos casos restantes (20%), en uno de ellos no fue posible evaluar la eficacia de tratamiento tópico debido al fallecimiento del paciente poco después de comenzar el tratamiento por la gravedad de su patología de base. En el otro caso, se optó por realizar un desescalado del tratamiento y modificar la colistina por gentamicina, ambas empleadas de forma tópica, al aislarse una cepa de P. aeruginosa con sensibilidad a gentamicina.
Ningún paciente desarrolló signos de toxicidad local ni sistémica al tratamiento tópico con colistina.
La mediana del tiempo a la erradicación fue de 3,5 semanas (IC 95%: 1-6).
DISCUSIÓN
El presente estudio trata de aportar información derivada de la práctica clínica respecto al tratamiento de la infección de las heridas crónicas, con aislamiento de bacterias gram-negativas resistentes a los tratamientos habituales.
Se consiguió una tasa de erradicación del 80% tras el empleo de crema de colistina al 0,1% para el tratamiento de las infecciones de heridas crónicas por microorganismos gram-negativos.
Algunas bacterias gram-negativas como A. Baumannii o P. aeruginosa presentan una gran facilidad para desarrollar resistencia a los tratamientos antibióticos habituales. Esta última, presenta un alto nivel de resistencia de forma intrínseca, además de una gran capacidad de adquirir mecanismos de resistencia, siendo habitual que cepas inicialmente sensibles se hagan resistentes a los pocos días de iniciar un tratamiento antibiótico. Además, hasta un 7% de personas sanas pueden ser portadoras de cepas resistentes en garganta, mucosa nasal y piel, y hasta un 24% en heces13-15.
Además, teniendo en cuenta los datos epidemiológicos del año 2015 de nuestro centro, la prevalencia de aislados de P. aeruginosa MDR así como XDR fue del 10%, con un perfil de sensibilidad que habitualmente solo responde a colistina.
Pese a la amplia experiencia existente en la práctica clínica en el manejo de las heridas crónicas, en la actualidad sigue existiendo controversia respecto al adecuado uso de antisépticos y/o antibióticos. En general, se desaconseja el tratamiento sistemático con antisépticos y/o antibióticos tópicos o sistémicos, recomendando su empleo únicamente en aquellos casos con presencia de infección confirmada16-20. A pesar de esto, algunos estudios2,3 muestran como hasta un 60-70% de los pacientes con algún tipo de herida crónica reciben al menos un tratamiento antibiótico sistémico.
El uso de sustancias con efecto antiséptico en el manejo de infecciones de heridas por P. aeruginosa y otros microorganismos, puede ayudar a evitar o limitar el uso de antibióticos. Por ejemplo el uso de ácido acético está descrito desde hace muchos años en pacientes con heridas de guerra por su poder bactericida. Se ha descrito su utilización a bajas concentraciones (1% al 5%) ya que en concentraciones superiores puede producir dolor y comezón, pero los datos sobre su uso proceden de estudios llevados a cabo en pacientes muy heterogéneos frente a infecciones por diversos agentes, entre los que se encuentran gérmenes gram-negativos como P. aeruginosa y Acinetobacter spp21. El mecanismo exacto por el que ejerce su efecto antiséptico es desconocido, aunque se le supone un efecto sobre la integridad de la pared celular21.
En nuestro centro se emplean soluciones de ácido acético al 3%, pero su uso se limita únicamente al cuidado de heridas superficiales ya que no está claro su posible efecto deletéreo en la cicatrización de las mismas. Al respecto, existen estudios in vitro donde se evalúa la potencial toxicidad de los agentes antisépticos sobre los fibroblastos y queratinocitos, lo que dificultaría la cicatrización de las heridas, por ello se sigue cuestionando su uso22.
Por tanto, debido a la elevada prevalencia de cepas resistentes a los tratamientos habituales observada en nuestro centro y a la escasez de alternativas terapéuticas, se planteó la necesidad de disponer de una fórmula magistral de colistina para su aplicación por vía tópica, especialmente destinada a aquellos casos con heridas profundas y extensas con criterios de infección definidos.
La administración tópica de antibióticos para el tratamiento de infecciones de heridas presenta ciertas ventajas frente al tratamiento sistémico, como su escasa toxicidad. Además, no es preciso mantener ingresado al paciente durante el tratamiento disminuyendo así el riesgo de desarrollar infecciones nosocomiales y el coste de la atención sanitaria proporcionada al paciente23.
En cuanto a la duración del tratamiento antimicrobiano, no existe consenso respecto a la duración óptima del mismo3,18. Para el manejo de las infecciones de úlceras de pie diabético, Lipsky et al.20 recomiendan mantener el tratamiento antibiótico hasta la completa resolución de los signos y síntomas de infección. En cambio, desaconsejan su mantenimiento hasta la cicatrización de las úlceras. Como recomendación en este tipo de heridas proponen un periodo de 1-2 semanas en caso de infecciones moderadas y de 2-3 en caso de infecciones más graves.
Los pacientes incluidos en nuestro estudio fueron tratados con colistina tópica, inicialmente con una duración indefinida hasta la erradicación de los microorganismos causantes de la infección, pero sujeta a la evolución clínica y microbiológica de la herida. Únicamente se observó un solo caso en el que, debido a la gravedad de su patología de base, la duración del tratamiento se prolongó durante 24 semanas a pesar de que la erradicación se consiguió a las 6 semanas.
Respecto al tiempo de evolución de las heridas, nuestro estudio muestra una gran disparidad. Tres pacientes destacaban por presentar heridas de larga evolución (24, 72 y 84 meses) que fueron tratadas previamente con diferentes antimicrobianos. En cuanto al resto de pacientes, el tiempo de evolución de las heridas estuvo comprendido entre 1 y 4 meses.
Durante el seguimiento posterior de los pacientes, en dos casos con infección previamente erradicada, se observó de nuevo crecimiento de P. aeruginosa XDR. Uno de ellos, con el mismo perfil de sensibilidad antibiótica, que no precisó tratamiento al no presentar signos de infección, mientras que el otro paciente fue tratado con ceftazidima (único antimicrobiano al que presentaba sensibilidad).
En cuanto al perfil de seguridad, algunos autores defienden que el tratamiento tópico presenta un bajo riesgo de seleccionar cepas resistentes, debido teóricamente a la elevada concentración de fármaco disponible en el foco de la infección y su alta permanencia en la zona afectada2.
Sin embargo, otros autores1,3,23 desaconsejan el uso rutinario de antibióticos tópicos debido al posible riesgo de producir hipersensibilidad retardada, superinfecciones y selección de microorganismos resistentes. Sin embargo, en nuestro estudio ninguno de los pacientes desarrolló toxicidad, reacciones de hipersensibilidad, ni se evidenció la selección de cepas resistentes al recibir tratamiento con la formulación tópica de colistina. Estos resultados sugieren que el manejo de infecciones de heridas crónicas con tratamientos antibióticos tópicos es seguro tanto para el paciente como a nivel epidemiológico, al no fomentar el desarrollo de resistencias.
Pese a los datos disponibles, debemos tener en cuenta las limitaciones del estudio, principalmente el bajo número de pacientes y la corta duración del mismo. Sin embargo, uno de los casos incluidos estuvo en tratamiento durante 6 meses consiguiendo la erradicación del microorganismo sin desarrollar toxicidades.
Otra limitación es la corta duración del seguimiento de los pacientes. La infección de las heridas se sabe que puede jugar un importante papel en la evolución de las mismas, dificultando su correcta cicatrización1,18. Por ello, sería interesante estudiar si aquellos pacientes en los que se logra erradicar la infección, presentan finalmente una correcta cicatrización.
CONCLUSIÓN
La aplicación tópica de colistina en crema puede ser una alternativa eficaz y segura para el tratamiento de la infección de heridas crónicas de diversa índole en aquellos pacientes que pese al correcto manejo de las mismas desarrollan infección por bacterias gram-negativas.
Financiación: Los autores declaran no haber recibido financiación para la realización de este estudio.
Aprobación ética: El estudio cuenta con la aprobación del Comité Ético de Investigación Clínica de Aragón (CEICA), que consideró que el consentimiento informado en este tipo de estudios no era necesario, asegurando en todo momento la confidencialidad total de los datos de los pacientes.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.
BIBLIOGRAFÍA
1. Siddiqui AR, Bernstein JM. Chronic wound infection: Facts and controversies. Clin Dermatol. 2010 Oct;28(5):519-26.
2. Howell-Jones RS, Wilson MJ, Hill KE, Howard AJ, Price PE, Thomas DW. A review of the microbiology, antibiotic usage and resistance in chronic skin wounds. J Antimicrob Chemother. 2005 Feb;55(2):143-9.
3. Landis SJ. Chronic wound infection and antimicrobial use. Adv Skin Wound Care. 2008 Nov;21(11):531-540; quiz 541-542.
4. Klein S, Schreml S, Dolderer J, Gehmert S, Niederbichler A, Landthaler M, et al. Evidence-based topical management of chronic wounds according to the T.I.M.E. principle. J der Dtsch Dermatologischen Gesellschaft = J Ger Soc Dermatology JDDG. 2013 Sep;11(9):819-29.
5. European Wound Management Association (EWMA). Position Document: Identifying criteria for wound infection. London: MEP Ltd, 2005.
6. Michalopoulos AS, Karatza DC. Multidrug-resistant Gram-negative infections: the use of colistin. Expert Rev Anti Infect Ther. 2010 Sep;8(9):1009-17.
7. Horcajada JP. Usefulness of PK/PD parameters of antimicrobials in the treatment of complex and extremely-resistant infections. Rev Española Quimioter. 2015 Sep;28 Suppl 1:16-8.
8. Falagas ME, Kasiakou SK, Saravolatz LD. Colistin: The Revival of Polymyxins for the Management of Multidrug-Resistant Gram-Negative Bacterial Infections. Clin Infect Dis. 2005 Jan;40(9):1333-41.
9. March Lopez P, Redondo Capafons S, Cruz Guerrero D, Garriga Biosca R. [Colistine 0,1% cream in the treatment of Pseudomonas aeruginosa multiresistant]. Farm Hosp. 2013 Aug;37(4):339-40.
10. González Contreras J, Galindo Rueda M, Mora Santiago M, Flores Cuellar M, Fuentes Ibáñez M, Sánchez Yáñez E. Crema de Colistina 0,1% en el tratamiento de infecciones locales por Acinetobacter baumanii. 54 Congr Soc Española Farm Hosp. Zaragoza, 2009.
11. Ministerio de Sanidad y Consumo. Formulario Nacional. Primera Ed. Madrid: Imprenta Nacional del Boletín Oficial del Estado; 2003.
12. Ministerio de Sanidad SS e I. Guía de buenas prácticas de preparación de medicamentos en servicios de farmacia hospitalaria. 2014.
13. Montero MM. Pseudomonas aeruginosa multiresistente: aspectos epidemiológicos, clínicos y terapéuticos. Universitat Autònoma de Barcelona; 2012.
14. Oliver A. Resistencia a carbapenemas y Acinetobacter baumannii. Enferm Infecc Microbiol Clin. 2004;22(05):259-61.
15. Hernández Torres A, García Vázquez E, Yagüe G, Gomez Gomez J. Acinetobacter baumanii multirresistente: situación clínica actual y nuevas perspectivas. Rev Esp Quim. 2010;23(1):12-9.
16. Association for the Advancement of Wound Care (AAWC). Association for the Advancement of Wound Care (AAWC) venous ulcer guideline. Malvern (PA) 2010.
17. Intercollegiate Guidelines Network S. Management of chronic venous leg ulcers Scottish Intercollegiate Guidelines Network. 2010;
18. O’Meara S, Al-Kurdi D, Ologun Y, Ovington LG, Martyn-St James M, Richardson R. Antibiotics and antiseptics for venous leg ulcers. Cochrane Database Syst Rev. 2014;1:CD003557.
19. National Institute for Health and Care Excellence (NICE). Pressure ulcers: prevention and management of pressure ulcers. 2014.
20. Lipsky BA, Berendt AR, Cornia PB, Pile JC, Peters EJG, Armstrong DG, et al. 2012 infectious diseases society of America clinical practice guideline for the diagnosis and treatment of diabetic foot infections. Clinical Infectious Diseases. 2012.
21. Ryssel H, Kloeters O, Germann G, Schäfer T, Wiedemann G, Oehlbauer M. The antimicrobial effect of acetic acid–an alternative to common local antiseptics? Burns [Internet]. 2009 Aug;35(5):695-700. Available from: http://www. ncbi.nlm.nih.gov/pubmed/19286325.
22. Nagoba BS, Selkar SP, Wadher BJ, Gandhi RC. Acetic acid treatment of pseudomonal wound infections–a review. J Infect Public Health [Internet]. 2013 Dec;6(6):410-5. Available from: http://www.ncbi.nlm.nih.gov/pubmed/23999348.
23. Lipsky BA, Hoey C. Topical antimicrobial therapy for treating chronic wounds. Clin Infect Dis. 2009 Nov;49(10):1541-9.
____